Medycyna regeneracyjna — komórki macierzyste i PRP
Medycyna regeneracyjna to jeden z najszybciej rozwijających się działów współczesnej medycyny. Jej celem nie jest jedynie łagodzenie objawów chorób, ale odbudowa uszkodzonych tkanek i narządów z wykorzystaniem biologicznych mechanizmów naprawczych organizmu. Dwie technologie przyciągają dziś szczególną uwagę badaczy i klinicystów: terapia komórkami macierzystymi oraz osocze bogatopłytkowe (PRP). Obie opierają się na potencjale regeneracyjnym własnych lub hodowlanych komórek — różnią się jednak mechanizmem działania, wskazaniami i stopniem klinicznego potwierdzenia skuteczności.
Jak działają komórki macierzyste w regeneracji tkanek
Komórki macierzyste to komórki zdolne zarówno do samoodnawiania, jak i różnicowania się w wyspecjalizowane typy komórek — mięśniowe, chrzęstne, nerwowe czy krwiotwórcze. Ta unikalna właściwość sprawia, że stanowią biologiczny materiał budowlany idealny do naprawy uszkodzeń, których organizm nie jest w stanie samodzielnie zrekompensować.
Wyróżniamy kilka klas komórek macierzystych stosowanych klinicznie. Hematopoetyczne komórki macierzyste, pozyskiwane ze szpiku kostnego lub krwi obwodowej, od dekad są standardem w leczeniu białaczek i chłoniaków. Mesenchymalne komórki macierzyste (MSC) izolowane ze szpiku, tkanki tłuszczowej lub łożyska wykazują szerokie działanie przeciwzapalne i immunomodulacyjne — to właśnie one stały się przedmiotem intensywnych badań w ortopedii, kardiologii i neurologii. Indukowane pluripotencjalne komórki macierzyste (iPSC), opracowane przez Shinyę Yamanakę w 2006 roku, umożliwiają przeprogramowanie dorosłych komórek somatycznych do stanu pluripotencji, co omija etyczne kontrowersje związane z komórkami embrionalnymi.
Mechanizm naprawczy — sygnalizacja parakrynna i zasiedlanie tkanek
Przez lata sądzono, że komórki macierzyste naprawiają tkanki przede wszystkim przez bezpośrednie różnicowanie i zastępowanie uszkodzonych komórek. Badania z ostatnich piętnastu lat istotnie zmodyfikowały ten obraz. Dominującym mechanizmem w wielu wskazaniach jest dziś sygnalizacja parakrynna — komórki macierzyste wydzielają cytokiny, czynniki wzrostu (m.in. VEGF, HGF, IGF-1) i egzosomy, które stymulują miejscowe procesy naprawcze, ograniczają stan zapalny i promują angiogenezę.
W kardiologii obserwuje się, że wstrzyknięcie MSC do mięśnia sercowego po zawale nie prowadzi do trwałego zasiedlenia tkanki przez nowe kardiomiocyty, lecz poprawia perfuzję i ogranicza przebudowę blizny przez wydzielane mediatory. Efekt jest mierzalny — w badaniach klinicznych frakcja wyrzutowa lewej komory poprawia się średnio o 3-5 punktów procentowych — choć skala tych korzyści jest nadal przedmiotem debaty.
Zastosowania kliniczne komórek macierzystych
Zakres potwierdzonych klinicznie zastosowań jest węższy niż sugerują popularne media, jednak systematycznie rośnie:
- Transplantacja hematopoetycznych komórek macierzystych w chorobach nowotworowych układu krwiotwórczego — standard leczenia od lat 70. XX wieku, rocznie przeprowadza się ponad 50 000 takich procedur na świecie.
- Leczenie ciężkich postaci stwardnienia rozsianego metodą AHSCT (autologiczna transplantacja HSC) — u pacjentów z aktywną postacią rzutowo-remisyjną wykazuje wyższą skuteczność niż klasyczne leki immunomodulacyjne.
- Terapia graftami chrzęstnymi wzbogaconymi MSC w zaawansowanej chorobie zwyrodnieniowej stawu kolanowego — badania fazy II i III wykazują redukcję dolegliwości bólowych o 40-60% po 12 miesiącach.
- Leczenie ran przewlekłych i odleżyn u pacjentów z cukrzycą — lokalne podanie MSC przyspiesza granulację i epitelializację w przypadkach opornych na standardowe metody.
Wyniki wymagają ostrożnej interpretacji — różnorodność protokołów, źródeł komórek i populacji pacjentów utrudnia bezpośrednie porównania między badaniami.
Osocze bogatopłytkowe — czym jest PRP i jak działa
Osocze bogatopłytkowe, znane pod skrótem PRP (z ang. platelet-rich plasma), to preparat uzyskiwany z krwi własnej pacjenta przez jej odwirowanie. Proces wirowania pozwala wyodrębnić frakcję osocza zawierającą płytki krwi w stężeniu 4-8-krotnie wyższym niż we krwi obwodowej — standardowo 150-350 tys./µl wzrasta do ponad 1 mln/µl.
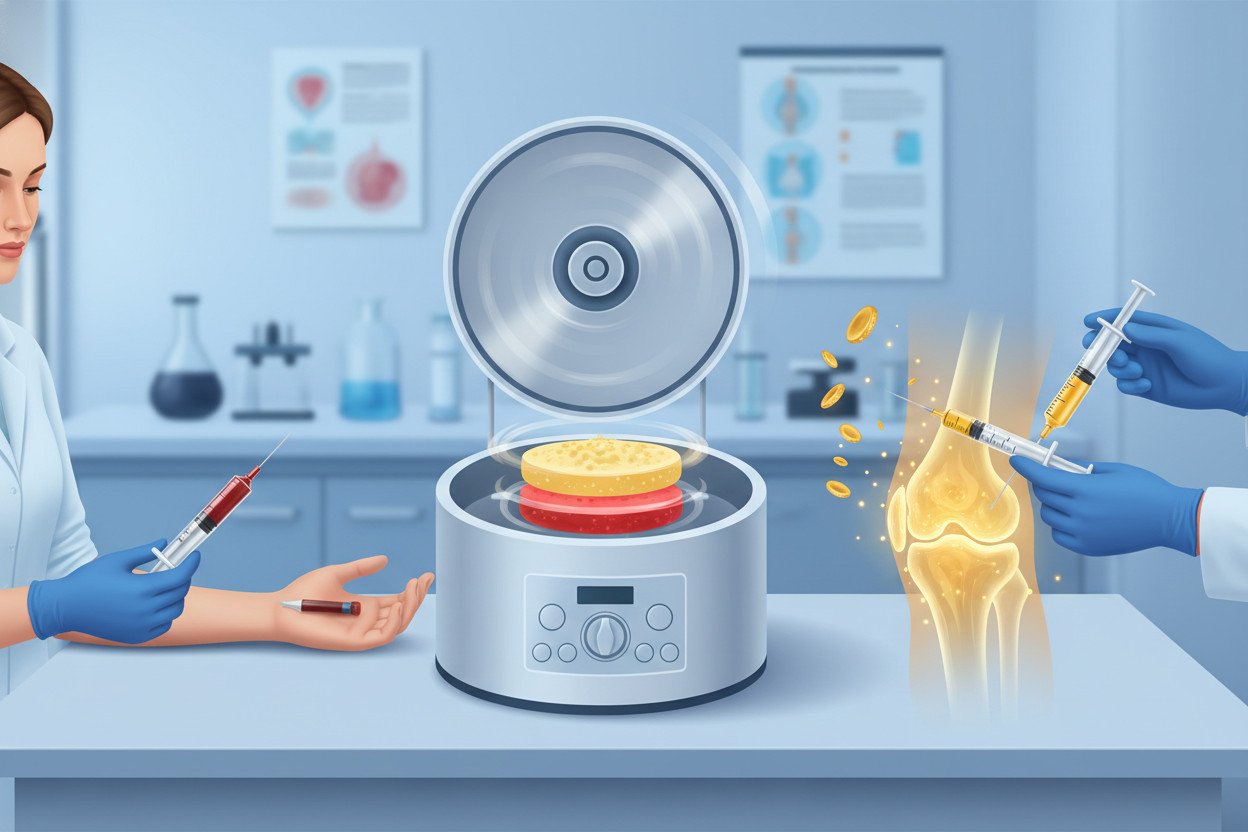
Mechanizm terapeutyczny PRP opiera się na degranulacji płytek i uwolnieniu alfa-granulek zawierających czynniki wzrostu: PDGF (płytkopochodny czynnik wzrostu), TGF-β, EGF, FGF oraz insulinopodobny IGF-1. Czynniki te stymulują proliferację fibroblastów, syntezę kolagenu, angiogenezę i chemotaksję komórek naprawczych do miejsca podania. Efekt pojawia się stosunkowo szybko — pierwsze zmiany w tkankach obserwuje się w ciągu 48-72 godzin od iniekcji.
Jak przebiega procedura pobrania i podania PRP
Procedura jest ambulatoryjna i trwa zazwyczaj 30-60 minut. Po pobraniu 20-60 ml krwi żylnej próbkę umieszcza się w specjalnych probówkach z antykoagulantem i wiruje w dwóch etapach — rozdzielając erytrocyty, warstwę trombocytów i osocze ubogopłytkowe. Uzyskany preparat można wzbogacić lub zubożyć o leukocyty, co zmienia jego profil działania: PRP leukocytarne (L-PRP) wykazuje silniejsze działanie przeciwdrobnoustrojowe, ale generuje silniejszy odczyn zapalny po iniekcji.
Podanie odbywa się pod kontrolą ultrasonografii — precyzja iniekcji istotnie wpływa na skuteczność. Efekt kliniczny nie jest natychmiastowy. W ortopedii pacjenci zazwyczaj wymagają serii 2-3 iniekcji w odstępach 2-4-tygodniowych, a pełna ocena wyników następuje po 3-6 miesiącach.
Zastosowania PRP w ortopedii, dermatologii i medycynie estetycznej
PRP znalazło zastosowanie w kilku obszarach klinicznych, choć poziom dowodów różni się między nimi.
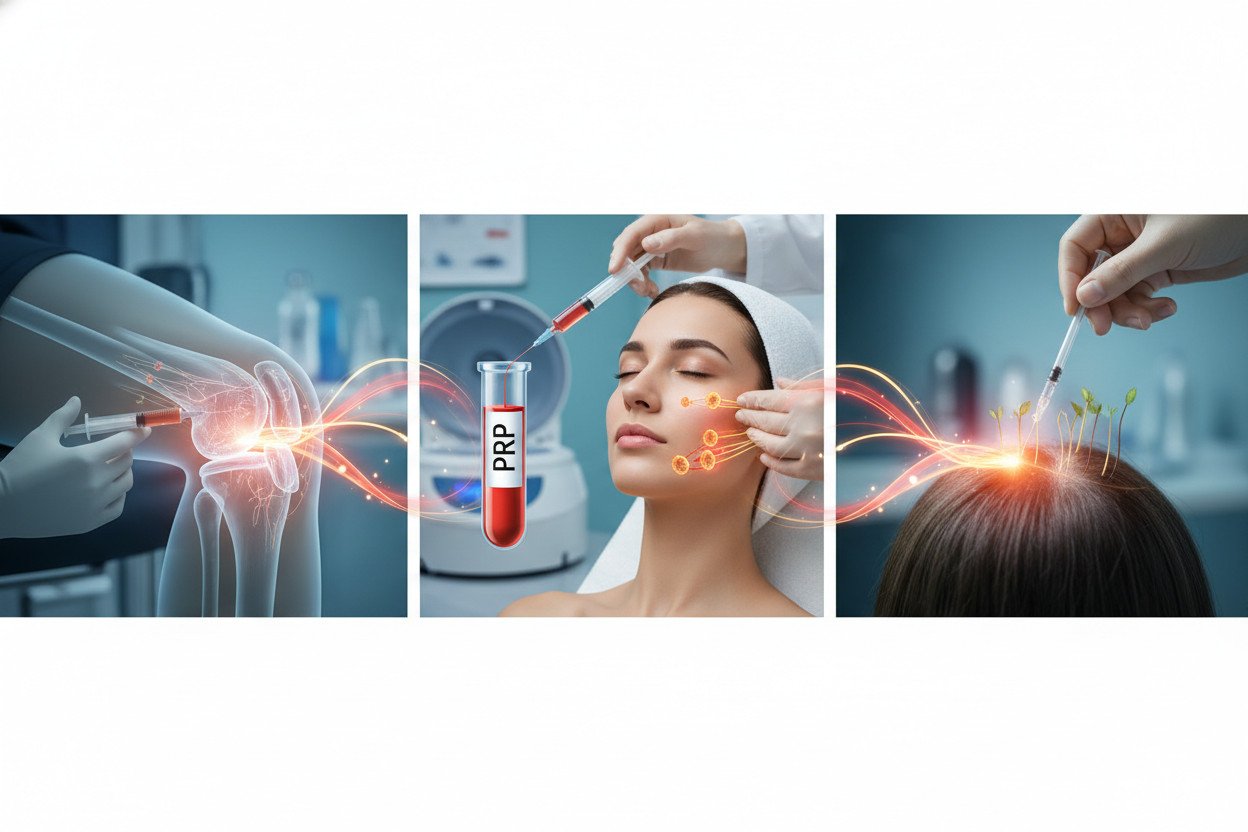
W ortopedii najlepiej udokumentowane są wskazania związane z tendinopatiami — szczególnie entezopatią ścięgna Achillesa i łokciem tenisisty. Metaanalizy obejmujące łącznie kilka tysięcy pacjentów wskazują na istotne zmniejszenie dolegliwości bólowych po 6 miesiącach w porównaniu z iniekcją kortykosteroidu lub soli fizjologicznej. Skuteczność w gonartrozie (chorobie zwyrodnieniowej stawu kolanowego) jest przedmiotem dyskusji — część badań wykazuje poprawę funkcjonalną i redukcję bólu porównywalną z kwasem hialuronowym, jednak wyniki nie są jednoznaczne, a efekt może ustępować po 12 miesiącach.
W dermatologii klinicznej PRP stosowane jest w leczeniu łysienia androgenowego. Protokół obejmuje iniekcje śródskórne w obszar czepca ścięgnistego, zazwyczaj co 4-6 tygodni przez 3-4 miesiące. Badania wykazują zwiększenie gęstości włosów i grubości łodygi w zakresie 20-30% po 6 miesiącach terapii — skuteczność jest wyższa we wczesnych stadiach wyłysienia.
Medycyna estetyczna to obszar, gdzie popularność PRP przerosła dowody naukowe. Zabieg zwany „wampirzym liftingiem” (połączenie mikroigłowania z podaniem PRP) cieszy się dużym zainteresowaniem, jednak wyniki kontrolowanych badań klinicznych są niejednoznaczne. Poprawa tekstury skóry i redukcja drobnych zmarszczek jest obserwowana, ale wielkość efektu jest skromna i zależy silnie od protokołu przygotowania preparatu.
- Entezopatia ścięgna Achillesa i łokieć tenisisty — najlepiej udokumentowane wskazanie w ortopedii.
- Choroba zwyrodnieniowa stawu kolanowego — skuteczność porównywalna z kwasem hialuronowym, efekt ustępuje po roku.
- Łysienie androgenowe — wzrost gęstości włosów o 20-30% po pełnym cyklu leczenia.
- Przewlekłe rany i owrzodzenia — stosowane jako uzupełnienie leczenia konwencjonalnego.
- Uszkodzenia mięśniowo-więzadłowe u sportowców — skrócenie czasu regeneracji, głównie w kontuzjach ścięgna rzepki.
Decyzja o zastosowaniu PRP powinna uwzględniać dokumentację kliniczną dla konkretnego wskazania, nie opierać się wyłącznie na ogólnym mechanizmie działania.
Medycyna regeneracyjna — ograniczenia, ryzyko i stan badań
Rosnąca popularność terapii regeneracyjnych sprawia, że wiele metod trafia do praktyki klinicznej szybciej, niż pozwalałby na to rygor badań randomizowanych. To istotny problem, który wymaga rzetelnej oceny zarówno po stronie lekarzy, jak i pacjentów.
Głównym ograniczeniem badań nad komórkami macierzystymi jest heterogeniczność preparatów — różne źródła komórek, metody izolacji, pasaże hodowlane i dawki utrudniają porównywalność wyników. Dodatkowym wyzwaniem są kwestie bezpieczeństwa: transplantacja allogenicznych komórek macierzystych wiąże się z ryzykiem choroby przeszczep przeciwko gospodarzowi (GvHD), a terapie oparte na iPSC niosą ryzyko tumorigenności wynikające z potencjalnej niestabilności genomu.
PRP jest metodą zasadniczo bezpieczną ze względu na autologiczny charakter preparatu — reakcje alergiczne praktycznie nie występują. Ryzyko infekcji przy zachowaniu standardów aseptyki jest śladowe, a najczęstszym działaniem niepożądanym jest miejscowy ból i obrzęk przez 48-72 godziny po iniekcji. Problemem jest brak standaryzacji — stężenie płytek, obecność leukocytów, pH preparatu i sposób aktywacji różnią się między ośrodkami, co uniemożliwia bezpośrednie porównywanie wyników badań.
Perspektywy na najbliższe lata
Medycyna regeneracyjna stoi u progu istotnych zmian metodologicznych. Rosnąca rola terapii egzosomami — bezkomórkowymi pęcherzykami zawierającymi RNA, białka sygnałowe i lipidy — może zastąpić lub uzupełnić klasyczne terapie komórkowe, eliminując część ryzyk związanych z podaniem żywych komórek. Technologia CRISPR/Cas9 otwiera możliwość edycji genów w komórkach macierzystych przed ich podaniem, co może dramatycznie poprawić bezpieczeństwo i precyzję terapii.
Regulacje prawne ewoluują — Europejska Agencja Leków (EMA) kategoryzuje terapie zaawansowane (ATMP) jako odrębną klasę produktów leczniczych podlegającą rygorystycznej procedurze dopuszczenia. Do 2024 roku zarejestrowanych zostało w Europie ponad 20 produktów ATMP, w tym kilka opartych na komórkach macierzystych. Liczba ta będzie rosła wraz z dojrzewaniem wyników długoterminowych badań klinicznych.
Pacjenci rozważający terapię regeneracyjną powinni weryfikować, czy proponowana metoda dysponuje dokumentacją kliniczną dla ich konkretnego wskazania, a nie jedynie ogólnym mechanizmem działania. Transparentna rozmowa z lekarzem specjalistą na temat poziomu dowodów, realnych oczekiwań i alternatywnych metod leczenia pozostaje warunkiem świadomej decyzji terapeutycznej.