Szczepionki mRNA — jak działają i jakie mają przyszłe zastosowania
Szczepionki mRNA zastosowania, które do niedawna istniały wyłącznie w niszowych laboratoriach, trafiły do globalnej świadomości w ciągu zaledwie kilku miesięcy. Pandemiczne szczepionki przeciwko COVID-19 były pierwszymi preparatami tego rodzaju zatwierdzonymi do powszechnego użytku — ale technologia, na której je oparto, ma znacznie starszą historię i znacznie szerszy potencjał. Dziś badacze z całego świata testują mRNA jako narzędzie w walce z nowotworami, chorobami autoimmunologicznymi i rzadkimi schorzeniami genetycznymi.
Żeby ocenić, dokąd ta technologia zmierza, trzeba najpierw zrozumieć, jak naprawdę działa.
Jak technologia mRNA programuje odpowiedź immunologiczną
Tradycyjne szczepionki dostarczają układowi odpornościowemu osłabiony patogen, jego fragment lub białko — coś, co układ immunologiczny może „zapamiętać”. Szczepionki oparte na mRNA technologia działają inaczej: zamiast samego antygenu wprowadzają instrukcję do jego produkcji.
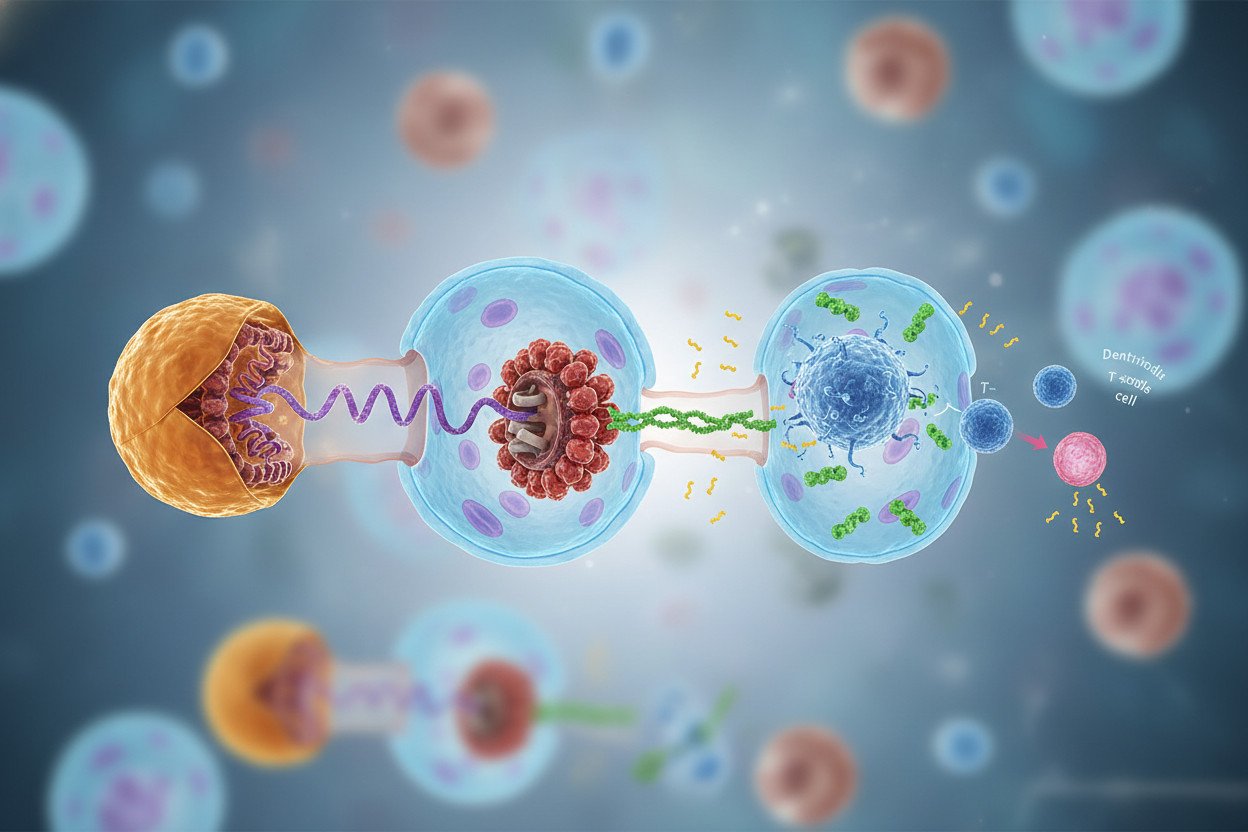
mRNA, czyli informacyjny kwas rybonukleinowy, to cząsteczka obecna w każdej żywej komórce. Jej naturalna rola polega na przenoszeniu kodu genetycznego z jądra komórkowego do rybosomów — tam DNA jest „tłumaczone” na białko. Szczepionka mRNA dostarcza sztuczną kopię takiej cząsteczki, zaprojektowaną tak, by rybosomy produkowały konkretne białko charakterystyczne dla patogenu — na przykład białko kolca koronawirusa SARS-CoV-2.
Po kilku dniach komórka rozkłada mRNA (podobnie jak rozkłada każdą inną cząsteczkę mRNA), a układ immunologiczny zdążył już rozpoznać wyprodukowane białko jako obce i wytworzyć przeciwciała. Co istotne, szczepionkowe mRNA nie trafia do jądra komórkowego i nie może integrować się z DNA — przemawia za tym zarówno mechanizm działania, jak i wieloletnie obserwacje kliniczne.
Lipidowe nanonaczynia — rozwiązanie problemu dostarczania
Przez dekady główna przeszkoda w praktycznym zastosowaniu mRNA nie leżała w samej cząsteczce, lecz w sposobie jej transportu do komórek. Nagie mRNA ulega szybkiej degradacji przez enzymy obecne w surowicy krwi — czas półtrwania bez ochrony wynosi zaledwie kilka minut.
Rozwiązaniem okazały się lipidowe nanocząsteczki (LNP — z ang. lipid nanoparticles). Są to mikroskopijne „kapsułki” zbudowane z tłuszczów, które otaczają cząsteczkę mRNA, chronią ją przed enzymami i ułatwiają wnikanie do wnętrza komórki przez fuzję z błoną komórkową. Skład lipidowy tych kapsułek był przedmiotem intensywnych badań przez co najmniej dwa dziesięciolecia zanim trafił do kliniki — nie był więc improwizacją przy pandemii. Odpowiedni dobór lipidów wpływa zarówno na stabilność preparatu, jak i na profil reakcji zapalnej po podaniu.
Modyfikacje nukleozydów a skuteczność i bezpieczeństwo
Drugim przełomem — nagrodzonym Nagrodą Nobla w 2023 roku — była obserwacja Katalin Karikó i Drew Weissmana, że zastąpienie naturalnej urydyny w cząsteczce mRNA zmodyfikowanym nukleozydem (pseudourydyną) drastycznie ogranicza wrodzoną odpowiedź zapalną organizmu. Niezmodyfikowane mRNA syntetyczne aktywuje receptory rozpoznające wzorce patogenów, wywołując silną reakcję odrzucenia — zanim komórka zdąży wyprodukować białko. Modyfikacja chemiczna pozwala „oszukać” te receptory, co jednocześnie poprawia wydajność translacji i bezpieczeństwo preparatu.
Szczepionka onkologiczna — mRNA w walce z nowotworami
Onkologia to obszar, w którym szczepionka onkologiczna oparta na mRNA wzbudza największe nadzieje — i gdzie postęp jest najbardziej widoczny. Nowotwory przez długi czas były poza zasięgiem szczepień, bo komórki rakowe wywodzą się z własnych komórek organizmu i są „niewidoczne” dla układu immunologicznego.

Indywidualizacja zmieniła tę perspektywę. Każdy guz nowotworowy posiada unikatowy zestaw mutacji somatycznych, które produkują białka nieobecne w zdrowych komórkach — tak zwane neoantygenów. Na podstawie sekwencjonowania genomu guza i algorytmów bioinformatycznych można zaprojektować indywidualną szczepionkę mRNA kodującą kilkanaście do kilkudziesięciu takich neoantygenów. Podana pacjentowi, „uczy” układ odpornościowy rozpoznawania i atakowania właśnie tych komórek.
Wyniki badań klinicznych fazy 2 z 2023 roku dla czerniaka (szczepionka mRNA-4157/V940 firmy Moderna we współpracy z MSD) pokazały, że połączenie personalizowanej szczepionki mRNA z immunoterapią pembrolizumabem zmniejszyło ryzyko nawrotu lub zgonu o 49% w porównaniu z samym pembrolizumabem. To wynik wystarczająco mocny, by uruchomić badania fazy 3 dla czerniaka i kilku innych typów nowotworów, w tym raka trzustki, płuca i jelita grubego.
Indywidualny charakter takich preparatów niesie jednak wyzwania logistyczne: czas od pobrania biopsji do dostarczenia szczepionki to obecnie 4-8 tygodni, a koszt produkcji pozostaje wysoki. Automatyzacja procesów bioinformatycznych i skrócenie łańcucha produkcji to kierunki, nad którymi intensywnie pracuje kilka zespołów równolegle.
Immunoterapia mRNA poza onkologią — nowe kierunki badań
Immunoterapia oparta na mRNA wychodzi poza ramy szczepień. W badaniach przedklinicznych i wczesnych fazach klinicznych pojawiają się zastosowania, które jeszcze dekadę temu byłyby uważane za spekulatywne.

Jednym z bardziej zaawansowanych kierunków jest terapia chorób autoimmunologicznych. W stwardnieniu rozsianym układ immunologiczny atakuje mielinę — osłonkę nerwów. Badania prowadzone przez BioNTech (od 2022 roku) testują mRNA kodujące fragmenty mieliny w strategii tolerancji immunologicznej: zamiast stymulować odpowiedź, celem jest jej wytłumienie wobec konkretnego antygenu własnego. To odwrócenie logiki tradycyjnych szczepień.
Innym obszarem są choroby rzadkie związane z deficytem enzymów. mRNA może dostarczyć tymczasową instrukcję produkcji enzymu, którego organizm nie wytwarza z powodu mutacji genetycznej. W odróżnieniu od terapii genowej (która modyfikuje DNA) podanie mRNA jest odwracalne i powtarzalne — co w przypadku chorób z charakterystyczną zmiennością nasilenia objawów może być zaletą.
Równolegle trwają badania nad szczepionkami profilaktycznymi przeciw wirusom HIV, RSV, metapneumowirusom i kilku szczepom grypy. Technologia mRNA pozwala szybko aktualizować sekwencję antygenu — co jest szczególnie ważne przy wirusach o dużej zmienności genetycznej.
- Szczepionki sezonowe z aktualizowaną co rok sekwencją antygenu — podobnie jak szczepionki na grypę, ale z szybszym cyklem produkcji
- Terapia zastępcza enzymów dla chorób rzadkich bez konieczności stałej modyfikacji genomu
- Szczepionki tolerogeniczne wyciszające autoagresję w chorobach takich jak cukrzyca typu 1 lub reumatoidalne zapalenie stawów
- Kodowanie przeciwciał neutralizujących bezpośrednio w komórkach — podejście określane jako „farmakologia mRNA”
Każde z wymienionych zastosowań jest na innym etapie gotowości klinicznej i wiąże się z odmiennymi wyzwaniami regulacyjnymi oraz dotyczącymi bezpieczeństwa długoterminowego.
Ograniczenia i wyzwania techniczne, których nie należy pomijać
Entuzjazm wokół mRNA jest uzasadniony danymi, ale uczciwy obraz wymaga wyraźnego zaznaczenia barier — zwłaszcza że kilka z nich wpływa na dostępność i bezpieczeństwo terapii.
Stabilność termiczna i dostępność w krajach o niskich dochodach
Preparaty mRNA wymagają przechowywania w niskich temperaturach. Szczepionki oparte na LNP były początkowo stabilne wyłącznie w temperaturze -70°C, co w praktyce ograniczało ich dystrybucję do placówek wyposażonych w specjalistyczny sprzęt chłodniczy. Nowsze formulacje — m.in. opracowane przez Moderna w 2022-2023 roku — zachowują stabilność przez kilka miesięcy w temperaturze 2-8°C, czyli w standardowej lodówce. To istotna zmiana, ale nadal niecałkowite rozwiązanie problemu dla krajów z ograniczoną infrastrukturą zimnego łańcucha dostaw.
Profil reakcji niepożądanych i monitoring długoterminowy
Lipidowe nanocząsteczki same w sobie mogą wywoływać odczyny zapalne — zarówno w miejscu podania, jak i ogólnoustrojowe. W przypadku szczepionek COVID-19 zaobserwowano rzadkie przypadki zapalenia mięśnia sercowego (zwłaszcza u młodych mężczyzn po drugiej dawce), szacowane na 1-4 przypadki na 100 000 dawek. Monitorowanie bezpieczeństwa długoterminowego trwa, a regulatorzy w USA i UE wymagają od producentów prowadzenia rozszerzonych rejestrów przypadków przez co najmniej 5-10 lat od autoryzacji.
Dla terapeutycznych zastosowań mRNA (powtarzane dawkowanie w terapii chorób przewlekłych) dane długoterminowe dopiero się gromadzą — i ten aspekt pozostaje otwartą kwestią naukową.
Bariera personalizacji przy nowotworach
Sekwencjonowanie guza, analiza bioinformatyczna i synteza indywidualnej szczepionki mRNA to proces kosztowny i czasochłonny. Przy nowotworach z szybką dynamiką wzrostu — jak rak trzustki — okno terapeutyczne może być wąskie. Badacze pracują nad skróceniem czasu produkcji do 2-3 tygodni przy zachowaniu wymagań GMP (Good Manufacturing Practice), ale nie jest to jeszcze standard kliniczny. Cena personalizowanej terapii mRNA szacowana jest obecnie na ponad 100 000 USD za kurs leczenia, co w perspektywie globalnej dostępności jest barierą trudną do zignorowania.
Perspektywa kolejnej dekady dla szczepionek mRNA
Technologia mRNA wchodzi w dojrzałą fazę rozwoju — nie jest już proof of concept, ale wciąż nie jest w pełni skalowalna klinicznie dla wszystkich planowanych zastosowań. Spodziewane kamienie milowe do 2030 roku obejmują wyniki badań fazy 3 dla personalizowanych szczepionek onkologicznych w co najmniej 4-5 typach nowotworów, a pierwsze zatwierdzenia regulacyjne mogą nastąpić już w 2026-2027 roku przy pozytywnych danych.
Równie ważna jest standaryzacja platform bioprodukcji. Kilka firm, m.in. BioNTech, Moderna i CureVac, inwestuje w zautomatyzowane moduły produkcji mRNA, które mają skrócić czas od zaprojektowania sekwencji do gotowego preparatu do 24-48 godzin. Gdyby to się udało, technologia mRNA stałaby się „platformą programowalną” — reagującą na nowe patogeny lub mutacje guza z szybkością niemożliwą dla żadnej wcześniejszej metody wytwarzania szczepionek.
Bardziej odległe, ale badane aktywnie, są terapie sercowo-naczyniowe: podanie mRNA kodującego VEGF (czynnik wzrostu naczyń) bezpośrednio do tkanki serca po zawale miokardium, by stymulować regenerację. Badania na modelach zwierzęcych dają wyniki obiecujące — przejście do fazy 1 u ludzi planowane jest przez co najmniej dwa niezależne zespoły w perspektywie 2025-2026.
Decydujące będzie to, czy przemysł zdoła pogodzić trzy napięcia: szybkość innowacji z rygorem danych bezpieczeństwa, personalizację z skalowalnością produkcji oraz wysoką cenę terapii z realnym dostępem pacjentów. Odpowiedź na te pytania zdecyduje, czy szczepionki mRNA staną się technologią transformującą medycynę, czy pozostaną narzędziem dostępnym tylko dla zamożnych systemów ochrony zdrowia.